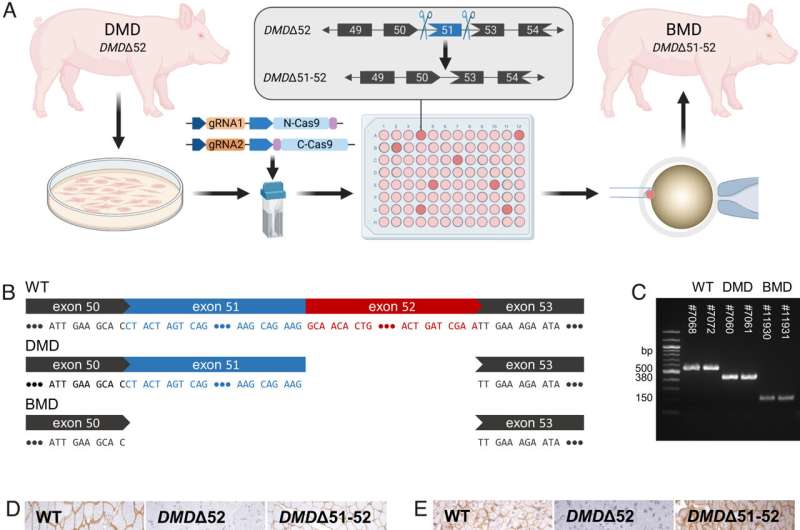
Generación y caracterización de DMDΔ51-52 animales. (A) Eliminación in vitro de DMD exón 51 en un porcino DMDLínea celular de riñón Δ52 mediante el sistema split-Cas9 mediado por inteína y posterior transferencia nuclear utilizando las células modificadas correctamente, seguida de transferencia de embriones a cerdas receptoras sincronizadas con el celo. (B y C) Secuenciación de Sanger (B) así como electroforesis de ADN en gel de agarosa (C) confirmaron la ausencia de los exones 51 y 52 en el ADNc generado a partir del ARNm de muestras de músculo tríceps braquial en DMDΔ51-52 animales pero no en DMDMuestras Δ52 y WT. (D y mi) Detección inmunohistoquímica de la proteína distrofina en el músculo tríceps (D) y (mi) miocardio. Barras = 100 µm. (F–I) Parámetros químicos clínicos en el suero sanguíneo: creatina quinasa (CK; F), creatinina (GRAMO), alanina aminotransferasa (ALT; H), y troponina I (I). Los gráficos muestran la mediana y el rango intercuartílico (npeso = 5, norte DMDΔ52 = 7, norteDMDΔ51-52 = 5 para F–H; nortepeso = 4, norte DMDΔ52 = 5, norteDMDΔ51-52 = 5 para I). Se indican las diferencias significativas: *PAG <0,05; **PAG <0,01; ***PAG < 0,001; y ns = no significativo. Crédito: procedimientos de la Academia Nacional de Ciencias (2023). DOI: 10.1073/pnas.2301250120
Un grupo de científicos de la Universidad Ludwig Maximilian dirigido por Eckhard Wolf ha desarrollado un modelo de DMD porcina con una mutación que imita las características de la enfermedad humana pero las desarrolla de forma acelerada. El estudio se publica en la revista procedimientos de la Academia Nacional de Ciencias.
La distrofia muscular de Duchenne (DMD) es una enfermedad mortal ligada al cromosoma X causada por mutaciones en el gen DMD, que provoca la ausencia total de distrofina y la degeneración progresiva de la musculatura esquelética y el miocardio. La mayoría de las mutaciones de DMD son deleciones de uno o más exones, con un punto de acceso en el rango de los exones 45 a 55. Las mutaciones de cambio de marco conducen a la formación de una distrofina truncada no funcional o a la ausencia total de distrofina debido a una distrofina prematura. codones de terminación y, como consecuencia, a distrofia muscular severa. Un ejemplo destacado es la pérdida del exón 52, que se asemeja a una de las mutaciones DMD más frecuentes en humanos.
El grupo Wolf ha desarrollado un modelo de DMD porcina con esta mutación, que imita las características bioquímicas, clínicas y patológicas de la enfermedad humana, pero las desarrolla de forma acelerada. En pacientes con DMD y en el modelo de cerdo correspondiente con una deleción del exón 52 de DMD (DMDD52), la expresión de una distrofina acortada internamente puede lograrse omitiendo el exón 51 de DMD para reformular la transcripción. Sin embargo, las estrategias actuales de administración de oligonucleótidos antisentido o herramientas de edición de genes limitan la omisión de exón a una proporción de (cardio-)miocitos; por lo tanto, el potencial terapéutico completo sigue sin estar claro.
Por lo tanto, el grupo de Wolf generó un modelo de corrección ubicua de la DMD mediante la eliminación sistémica del exón 51 en el modelo de cerdo distrófico que carece del exón 52 de la DMD. meta relevante. Debido a la alta susceptibilidad de los cerdos a las lesiones musculares distróficas, los cerdos DMDD51-52 que se asemejan a una forma de distrofia muscular de Becker (BMD) descubrirán resultados a largo plazo dentro de un marco de tiempo razonable.
Este nuevo estudio demuestra que los modelos de cerdos genéticamente adaptados no solo son útiles para estudiar los mecanismos de la enfermedad, sino también para predecir los mejores resultados posibles de las terapias dirigidas.
Más información:
Michael Stirm et al, La eliminación sistémica del exón 51 de DMD rescata la distrofia muscular de Duchenne clínicamente grave en un modelo de cerdo que carece del exón 52 de DMD, procedimientos de la Academia Nacional de Ciencias (2023). DOI: 10.1073/pnas.2301250120
Citación: Predicción del potencial terapéutico en la distrofia muscular de Duchenne usando un modelo animal (2023, 13 de julio) recuperado el 13 de julio de 2023 de https://medicalxpress.com/news/2023-07-therapeutic-potential-duchenne-muscular-dystrophy.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.


